本文作者:云也
一款药,4 个月前靠低价杀出重围,成为仿制药黑马;4 个月后,却被医保直接「拉黑」了。
这款药,就是 Dr. Reddy's 的盐酸托莫西汀胶囊。
昨晚,国家医保局公布重磅消息,第九批国采中刚刚中标这款药,因被查出原料药管理、工艺验证、质量控制等方面存在缺陷,取消中选资格,暂停进口、销售、使用。
生产企业也随即列入违规名单,暂停一年半国采的申报资格。国家医保局也提醒主供省份需要当即启动备供公司保障供应。[1]

▲上下滑动查看全文 图源:国家医保局官网
仿制药崛起,靠超低价挤走原研?
礼来公司原研的盐酸托莫西汀,是第一个被批准用于治疗多动症(注意缺陷多动障碍,ADHD)的非兴奋型药物,2002 年 7 月 27 日获得美国 FDA 批准上市销售。
2016 年,该药胶囊剂型获批在中国上市,并被收入 2017《国家医保药品目录》。
2018 年 9 月盐酸托莫西汀口服溶液剂型在中国获批,是《中国注意缺陷多动障碍防治指南(第二版)》非中枢兴奋剂类主要推荐药物。
但此时,原研礼来的使用方法专利(US-05658590)已经于 2017 年 5 月到期,胶囊和口服溶液的仿制都已如火如荼。
此时美国也已批准首个仿制药 图源:FDA 官网
ADHD 在我国学龄儿童的总患病率为 3~10%,成人发病率为 4~5%,都是相当高的发病率。由于有些患者对于兴奋类药物反应不佳,加上兴奋类药物需要严格管制,没有兴奋感更适用于合并抽动障碍的患儿,托莫西汀成了指南的主要推荐 [2]。
盐酸托莫西汀在第九批国采时第一次进入集采名录,而且直接成为竞争最激烈的品类之一。
当时,除了原研的礼来,胶囊剂型还有 5 家仿制药企业的 12 个批号获批生产,另有 3 家仿制申请在审评中;口服溶液有 8 家仿制药企业的 8 个批号获批生产,20 多家申请在审。
原研的 10mg 胶囊约 15 元/颗,25mg 约 20 元/颗,40mg 约 30 元/颗。而仿制药单价要低得多。很显然,国内各企业,和来自印度的仿制药企 Dr. Reddy's Laboratories Ltd.(也就是这次被严惩的药企),必然带来价格大战,对原研药造成重压。
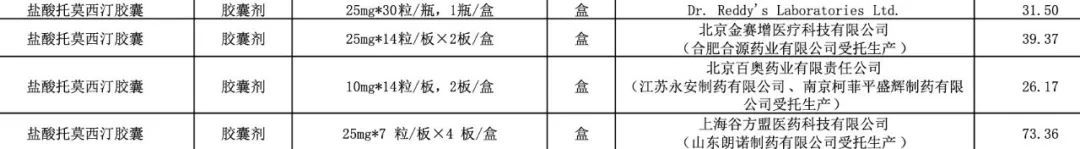
图源:资料 3
最终结果,也确实如此。
原研的选择,to be or not to be
而就在集采落选的同期,礼来在答患者问过程中流出的一封关于撤网申请引爆了网络。申请称,礼来因产品线战略调整,公司的择思达胶囊 2024 年 1 月底终止在华供应,10mg、25mg 和 40mg 三种全部停止。
礼来中国官网上个月的更新之后,产品名录中也直接撤下了择思达胶囊剂型 [4]。

中国当前产品已无盐酸托莫西汀胶囊剂型 图源:礼来中国官网
在刚刚宣布撤出时,「断货」通知疯传,甚至引发过抢购热潮,虽然对于中国患者群体,只是失去了一种药物选择,但对原研产品的信任和因此带来的偏好,确实客观存在。
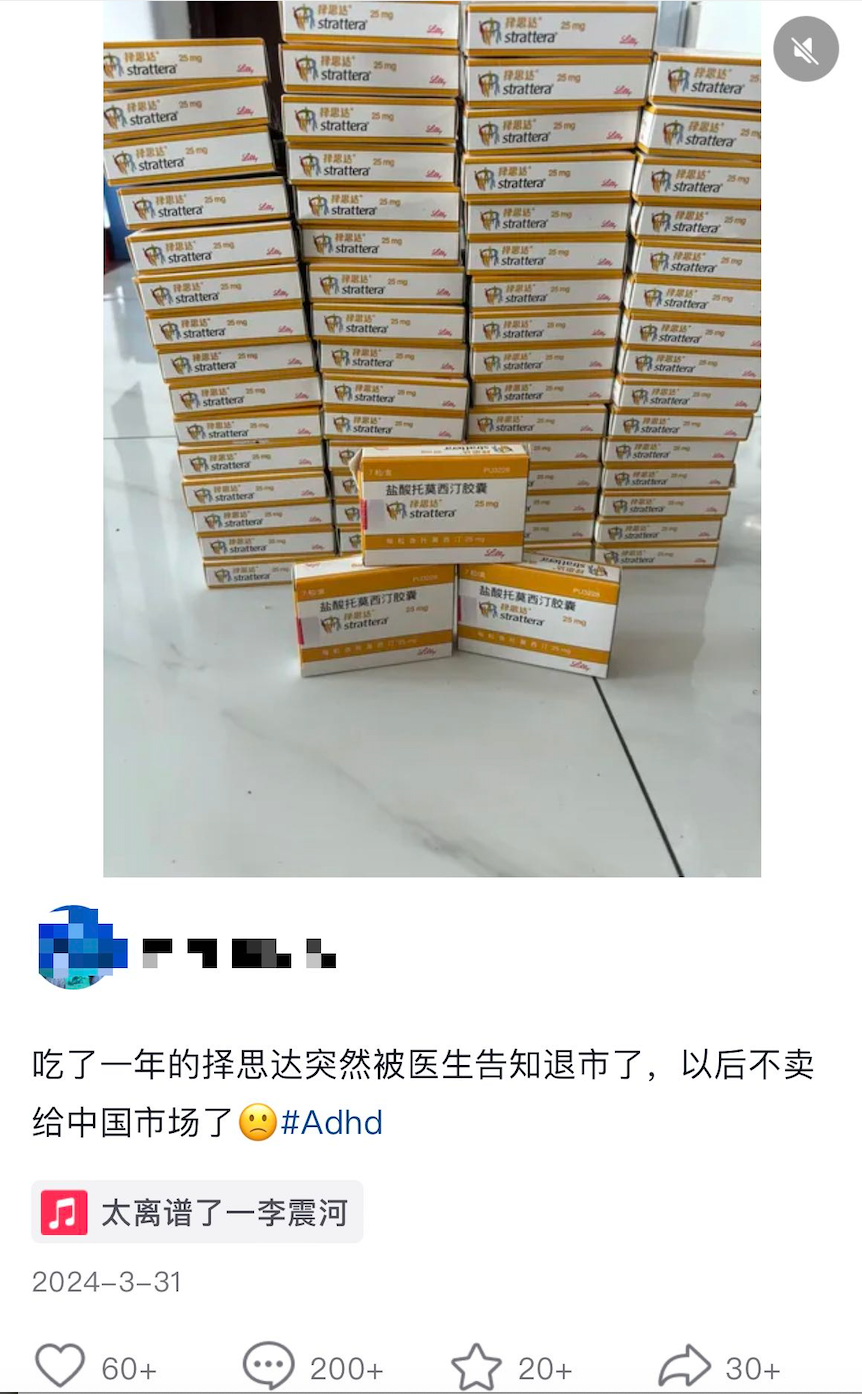
图源:社交媒体
因为原研药的撤出中国和第九批集采落选时间上的契合,让许多人直接认定原研药撤出中国市场,就是因为集采中被国产仿制药挤掉了。
但这样简单粗暴的归因不免有失偏颇。原研药的退出,是一道市场的选择题。
首先,专利保护期一过,原研药的销售受到仿制药冲击,是每一种原研药,在全世界每一个国家都必然经历的过程。作为世界顶级的超级大药企,在择思达身上,礼来自然也早就预见到了这一点,在财报中做出了公告,也很早就开始战略性调整,应对以减少对自己在神经疾病市场地位的冲击 [5]。

图源:资料 5
或许是出于多动症领域对于礼来的战略价值评估,礼来在多国都选择陆续停产择思达。
择思达最后一次出现在礼来财报中是 2020 年,礼来表示择思达因受仿制药冲击销量下降带来的影响,已被其他药物冲抵。
此后几年财报中就不再提及择思达,在其美国官网,择思达也从当前产品页面,被挪到了历史药品页面 [6]。
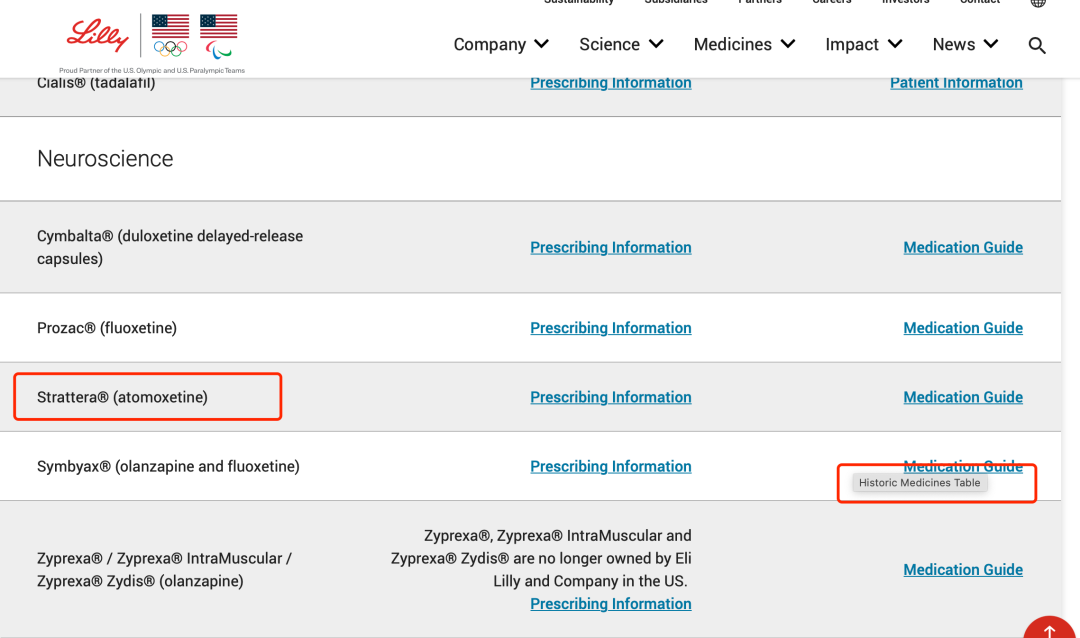
择思达已被列在 Historic Medicines 页面,而非当前产品
图源:礼来美国官网
而相对于直接放弃的胶囊剂型,口服溶液可依据患者体重调整剂量、服用方便,尤其对吞咽困难或低龄儿童有治疗优势。因为相对的差异化,口服溶液剂型成为礼来相对滞后放弃的部分,在国内仍有销售 [4]。
官方多次强调:仿制不能光顾着便宜
此次关于取消 Dr. Reddy's Laboratories Ltd. 盐酸托莫西汀胶囊中选资格并将该企业列入违规名单的公告中,国家医保局披露:
经国家药监局检查,该盐酸托莫西汀胶囊在原料药管理方面存在严重缺陷,未采取有效措施确保所使用原料药的有效期符合我国注册要求,另外在工艺验证、质量控制等方面存在缺陷,不符合我国《药品生产质量管理规范(2010 年修订)》要求。
2024 年 8 月 30 日,国家药监局发布公告,暂停进口、销售和使用该产品 [7]。

图源:国家药监局
在集采话题之下,「价廉」是否会导致低质,一直是全民关注的焦点,国家医保局也多次做出过回应。
集采的政策要求是「质优价宜」,目前采取的是以一致性评价作为质量入围门槛、持续开展中选药品质量监管的保障措施。国家医保局多次表示,集采中选国产仿制药是与原研药药学等效和生物等效的好药,且越来越多的真实世界证据表明它们在临床实践中与原研药品具有治疗等效性 [8]。
此番对于集采药品质量问题进行严惩,对于药企之间的价格竞争也是一次引导。
此次公告中国家医保局还提示,由该印度公司作为盐酸托莫西汀胶囊主供企业的省份,应启动替补程序,由备供企业替补成为主供企业,并按本企业中选价格供应;当备供企业不能满足供应需求时,由所在省份启动增补备供企业供应流程 [1]。
市场腾出来了,又有新的机会。但无论是怎样的仿制药、多么便宜,质量,永远应是竞争的底线。
策划:云也|监制:z_popeye、carollero
编辑:ifhealth 来源:丁香园
