3 月 10 日,艾伯维利生奇珠单抗注射液获 NMPA 批准上市,用于治疗成人中度至重度克罗恩病。
据官网显示,这是全球首个获批用于中重度活动性克罗恩病成人患者的白介素-23 抑制剂,也是国内首个拥有随身给药器的白介素-23 抑制剂。

图源:艾伯维官网
利生奇珠单抗(Risankizumab,Skyrizi)是一种 IL-23 抑制剂,通过与 IL-23 p19 亚基结合来选择性阻断 IL-23 介导的一系列免疫炎症反应。
利生奇珠单抗最初由勃林格殷格翰研发,2016 年艾伯维获得其开发和全球商业化权益,2019 年 3 月率先在日本获批上市。
截至目前,该药已在全球获批多项适应症:克罗恩病、斑块状银屑病、泛发性脓疱型银屑病、红皮病型银屑病和银屑病关节炎等。
在国内,利生奇珠单抗注射液和皮下注射液第二项上市申请获 CDE 受理(受理号:JXSS2400045/46/47),据 Insight 数据库推测申报的适应症为溃疡性结肠炎。
克罗恩病是一种慢性炎症性肠病,近年来,我国克罗恩病发病率呈快速上升趋势,从 1/100 000 上升到 20/100 000,如今已经成为国内常见的消化系统疾病之一。克罗恩病病程较长,易反复发作,迁延不愈,给患者带来长久的痛苦和工作生活上的不便。
据 Insight 数据库,目前国内已批准多款生物制剂用于治疗克罗恩病,如靶向 TNF-α 的阿达木单抗、英夫利西单抗,靶向 IL-12/23 的乌司奴单抗、靶向 α4β7 整合素的维得利珠单抗。此外,JAK 抑制剂乌帕替尼也在国内获批用于治疗克罗恩病。
利生奇珠单抗 III 期临床取得优效结果
2023 年 9 月,利生奇珠单抗 vs 乌司奴单抗治疗中重度克罗恩病的 III 期临床研究 SEQUENCE 取得积极顶线结果。
该研究达到两个主要终点:利生奇珠单抗组患者的临床缓解率非劣效于乌司奴单抗组(59% vs. 40%);内镜缓解率优效于乌司奴单抗组(32% vs. 16%,P<0.0001)。此外,利生奇珠单抗在该研究的所有次要终点上,与活性对照组相较均达到统计学显著性的优效性。
安全性方面,利生奇珠单抗的安全性与既往研究中观察到的情况一致,没有发现新的安全风险。
国产 IL-23 新药竞争相对缓和
此前,国内已批准 3 款 IL-23 新药,分别为强生的古塞奇尤单抗/乌司奴单抗和康哲药业引进的替瑞奇珠单抗。
其中古塞奇尤单抗和替瑞奇珠单抗均作用于 IL-23 p19 亚基,目前国内已获批用于斑块状银屑病;乌司奴单抗是通过结合 IL-12/23 的 p40 亚基发挥作用,目前已在国内获批两个适应症:斑块状银屑病和克罗恩病。
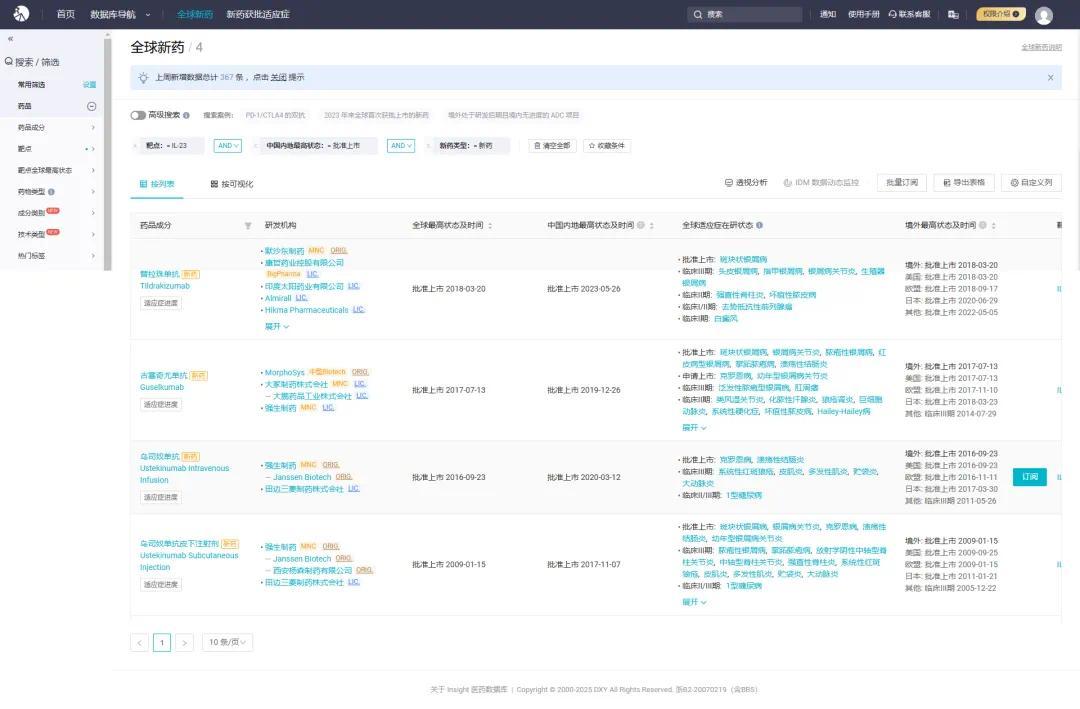
图源:Insight 数据库
据 Insight 数据库,目前国产 IL-23 靶向药的管线共有 13 款,其中 11 款处于活跃状态,竞争相对缓和。
针对 IL-12 p40 亚基的国产在研药物中,荃信生物的乌司奴单抗生物类似药 QX001S 已经于 2024 年 10 月在国内获批上市。
此外还有两款乌司奴单抗的类似药已经报上市,分别为百奥泰的 BAT2206 和石药集团的 SYSA 1902。在新药方面,康方生物的依若奇单抗进展最快,已经在国内报上市。
针对 IL-23 p19 亚基的国产在研药物相对比较少,其中进展最快的是信达生物的匹康奇拜单抗,已经申报上市;荃信生物的 QX004N 处于 II 期临床,石药集团的 NBL-012 处于 I 期临床。
编辑:vvy
编辑:vvy
| 分享到: |
上一篇 下一篇
