引言
埃万妥单抗(Amivantamab)是一种用于治疗 EGFR 外显子 20 插入突变晚期非小细胞肺癌(NSCLC)的 EGFR-MET 双特异性抗体。基于一项随机、开放标签的多中心 PAPILLON 研究,2024 年 3 月 1 日,FDA 批准埃万妥单抗联合卡铂和培美曲塞用于携带 EGFR 外显子 20 插入突变的局部晚期或转移性 NSCLC 患者的一线治疗,EGFR 外显子 20 插入突变二线治疗由快速获批转为晚期获批。
拉泽替尼(Lazertinib)是韩国柳韩洋行(Yuhan)研发的三代 EGFR-TKI,具有激活 EGFR 突变、靶向 T790M 突变的作用,在中枢神经系统(CNS)受累的 NSCLC 患者中具有强活性。2021 年韩国食品药品管理局批准拉泽替尼用于既往接受过 EGFR-TKI 治疗的 EGFR T790M 突变阳性局部晚期或转移性非小细胞肺癌患者的治疗。
本次 ASCO 年会公布了埃万妥单抗皮下(SC)vs. 静脉注射(IV)联合拉泽替尼用于治疗 EGFR 突变晚期非小细胞肺癌耐药后患者的全球 III 期随机对照试验 PALOMA-3 研究结果,公布的内容包括研究的总生存期(OS)结果。
研究背景
埃万妥单抗联合拉泽替尼在 EGFR 突变晚期 NSCLC 患者中展现出良好的抗肿瘤活性,而早期的临床研究显示埃万妥单抗(皮下)给药时间仅为 7 分钟,输液反应发生率较低,具有良好的耐受性。本次会议公布 PALOMA-3(NCT05388669)研究评估了埃万妥单抗(皮下或静脉注射)+ 拉泽替尼治疗方案在已使用奥希替尼和含铂化疗耐药后的 EGFR 19del/21L858R 晚期 NSCLC 患者的药代动力学参数(PK)、疗效和安全性。
研究方法
PALOMA-3 研究是一项国际多中心 3 期临床研究,旨在评估埃万妥单抗皮下(SC)vs. 静脉注射(IV)联合拉泽替尼治疗 EGFR 突变的晚期非小细胞肺癌一线治疗耐药后患者的药代动力学、疗效和安全性。入组的 EGFR 19del/21L858R 晚期 NSCLC 耐药后的患者 1:1 随机分配至埃万妥单抗皮下组(SC)和埃万妥单抗静脉注射组(IV)。
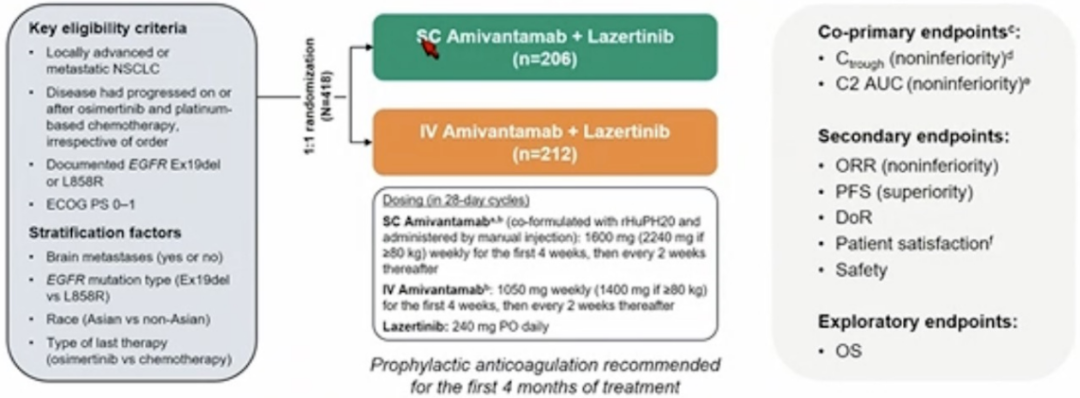
图 1:PALOMA-3 研究设计
埃万妥单抗皮下组采用方案为 1600 mg(2240 mg,≥80 kg)前 4 周每周 1 次 → 每 2 周 1 次 + 拉泽替尼 240 mg qd;
埃万妥单抗静脉注射组采用方案为 1050 mg(1400 mg,≥80 kg)前 4 周每周 1 次 → 每 2 周 1 次 + 拉泽替尼 240 mg qd。
两者的联合非劣效主要终点药代动力学通过两者血药浓度测定评估第 2 周期第 1 天(C2D1)或第 4 周期第 1 天(C4D2)的峰谷浓度和第 2 周期后的曲线下面积(AUC d1-15)。次要终点包含客观缓解率(ORR)、无进展生存期(PFS)、安全性等。探索性终点为总生存期(OS)。
研究结果
418 名入组的患者随机分配到皮下注射组(206)和静脉注射组(212),其中 416 例患者接受过至少一次治疗,患者中位年龄 61 岁,67% 为女性,61% 为亚裔,患者既往接受治疗的中位线数为 2。
中位随访 7.0 个月。主要终点药代动力学(PK)方面,皮下注射组和静脉注射组在 C2D1 峰谷血药浓度的几何平均比率(GMRs)为 1.15(90%CI:1.04–1.26);C4D1 峰谷血药浓度的 GMRs 为 1.43(90%CI:1.27–1.61);AUC d1-15 的 GMRs 为 1.03(90%CI:0.98–1.09),研究结果符合非劣效标准。
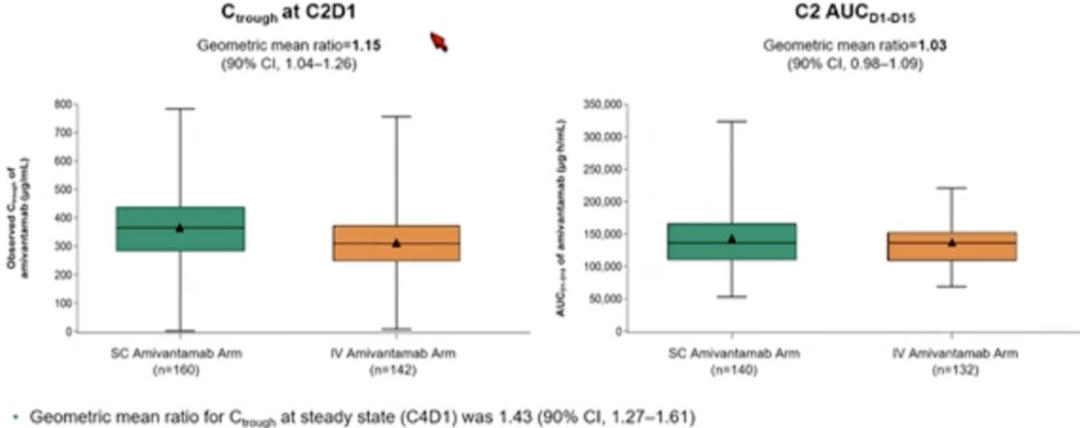
图 2:研究主要终点药代动力学结果
次要终点方面,皮下注射组和静脉注射组的 ORR 分别为 30.1% vs. 32.5%(RR 0.92;P = 0.001),符合非劣效标准,而中位缓解时间(DoR)方面,皮下注射组优于静脉注射组(11.2 vs. 8.3 个月);PFS 方面,皮下注射组相比静脉注射组有良好的获益趋势,中位 PFS 为 6.1 vs. 4.3 个月(HR 0.84;P = 0.20)。
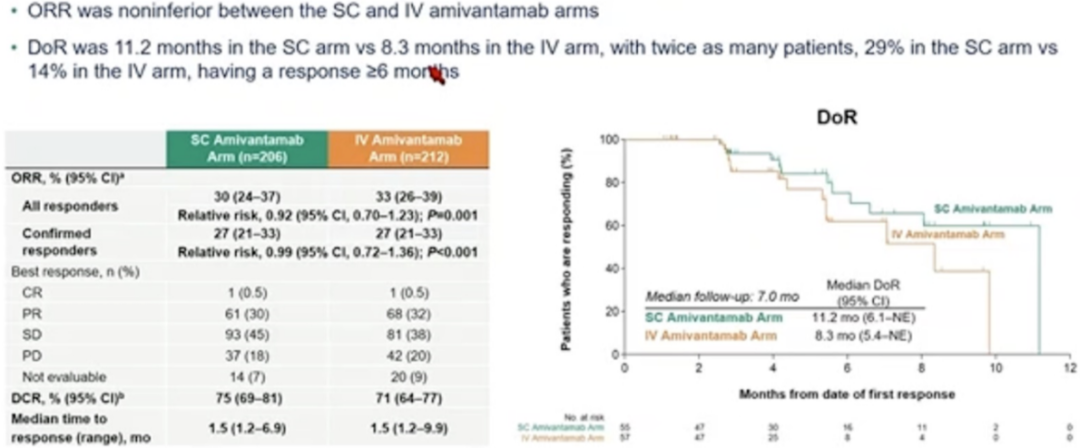
图 3:研究次要终点 ORR 和 DOR 结果
探索性终点 OS 方面,皮下注射相比静脉注射显著延长了患者的 OS(HR 0.62;95%CI:0.42–0.92;nominal P = 0.017),12 个月的 OS 率为 65% vs. 51%。
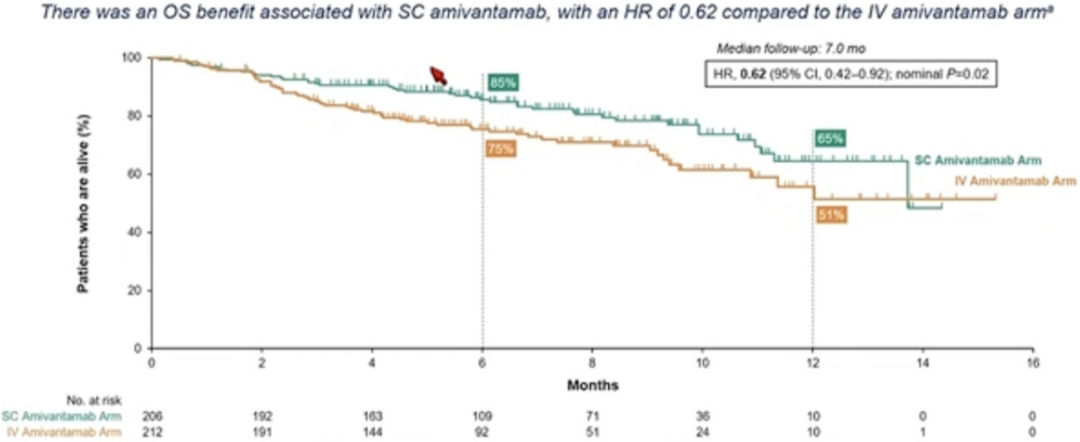
图 4:研究探索性终点 OS 结果
安全性方面,皮下注射组的输液反应发生率仅为静脉输液组的 1/5(13% vs. 66%),两者均主要为 1-2 级轻度输液反应(≥3 级 0.5% vs. 4%)。VTE 方面,入组患者中 81% 患者接受了预防性抗凝治疗,接受预防抗凝治疗患者 VTE 发生率为 10%,未接受预防抗凝治疗患者 VTE 发生率为 21%,皮下注射组和静脉注射组 VTE 报告率为 9% vs. 14%。抗凝治疗安全性良好,重度出血风险较低(1%,≥3 级)。
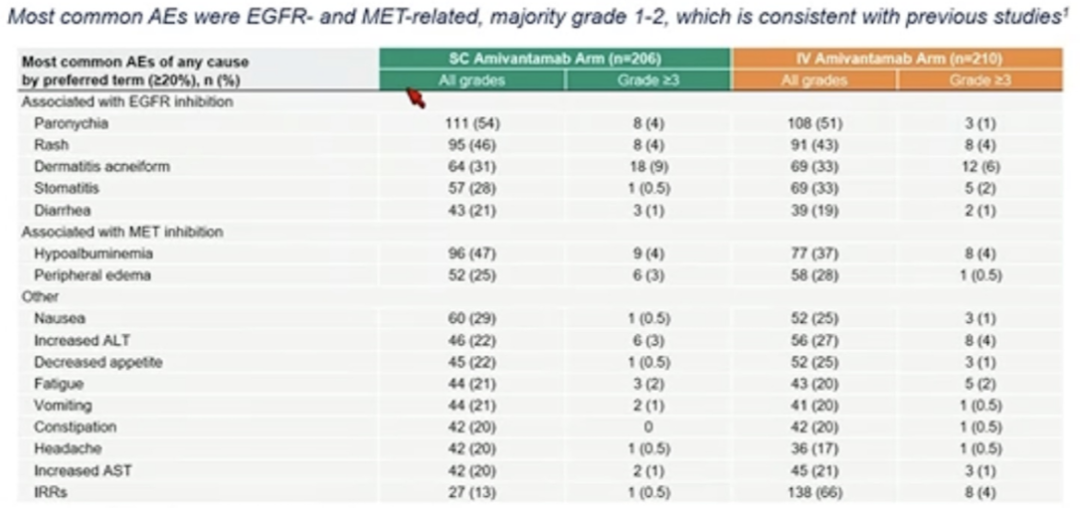
图 5:研究主要不良反应结果总结
研究结论
埃万妥单抗(Amivantamab)皮下注射和静脉注射在 EGFR+ mNSCLC 耐药患者中展现出相似的药代动力学和客观缓解率,而在 DoR 和 PFS 方面,埃万妥单抗皮下注射展现出获益趋势,OS 则显著获益,研究结果提示埃万妥单抗注射剂型和给药途径可能会影响患者的疗效。安全性方面,埃万妥单抗皮下注射安全性有所改善,输液反应和 VTE 发生率较低,预防性抗凝治疗安全性良好并有效降低 VTE 风险。另外,埃万妥单抗皮下注射仅需 5 分钟,而静脉注射需 2-5 小时,给药时间大幅缩短使更多患者认可其给药方便性,提高了患者的满意度和依从性。
整理:毛阳;编辑:lsh
编辑:lsh
| 分享到: |
上一篇 下一篇
