短短几年,人乳头瘤病毒(HPV)预防性疫苗从蓝海卷成红海:二价降至一杯奶茶钱,九价即将密集上市,激烈竞争已成定局。
HPV预防性疫苗这边卷得不可开交,宫颈癌仍是全球范围内的重大公共卫生挑战,在女性常见癌症中位列第四。2022年,全球估计新增66万例病例,并导致约35万例死亡,其中中国估计新确诊15.1万例宫颈癌患者,病例数约占全球总数的五分之一。
这主要有两方面原因:一是预防性疫苗的实际覆盖率仍不足,二是现有的预防性疫苗仅能预防感染,对于已感染且进展至癌前病变的患者并无治疗作用。
宫颈癌前病变,是宫颈细胞在受到高危型HPV病毒,特别是HPV-16型和HPV-18型病毒持续感染后,发生的一种在组织学上的高级别病理改变,包括CIN2级和CIN3级,若不及时治疗,进展为宫颈癌的风险会显著增加。
目前,宫颈癌前病变的治疗方案以手术为主,包括宫颈环形电切术(LEEP)和宫颈冷刀锥切术等。后者常用于范围较大或疑似更重的病变,但存在明显局限——无法彻底清除病毒,复发风险高,手术会破坏宫颈结构甚至导致全子宫切除,严重影响生育健康。
如今,一批HPV 治疗性疫苗正在试图解决这一难题。
根据摩熵医药数据库统计,全球处于临床阶段用于癌前病变的HPV治疗性疫苗有几十款,其中大部分尚处于早期临床阶段。目前只有基于DNA技术平台的HPV治疗性疫苗VGX-3100已进入III期临床研究。作为东方略引进的核心产品,VGX-3100在中国宫颈癌前病变患者中进行的III期临床研究的主要疗效和安全性数据将于2026年上半年公布, 成为该领域具有标志性进展的项目之一。鉴于宫颈癌前病变目前全球缺乏有效的非手术治疗方案,若VGX-3100能早日获批上市,广大癌前病变患者将有机会通过简单肌肉注射实现病毒清除和病变组织恢复,避免手术的痛苦。
在中国III期临床的关键阶段,1月28日,制药巨头A股和港股两地上市公司复星医药成员企业复星万邦就VGX-3100与东方略签订CSO、CDMO独家合作协议。复星万邦同意向东方略支付首付款和里程碑累计8亿元人民币,以及两位数的销售收入分成,以此获得VGX-3100在大中华区的独家商业化权益。
复星医药在临床关键阶段投出的这张“信任票”,为即将撞线的东方略,注入了强劲的商业化信心。
01 全球进展最快的疫苗
2008年,德国病毒学家哈拉尔德·楚尔·豪森荣获诺贝尔医学奖。这一荣誉归功于他在1976年提出的“HPV可能是宫颈癌病原体”的开创性假说,该假说最终被证实,革新了人们对宫颈癌病因的认知,也激发了生物医药企业对HPV疫苗的研发热情,Inovio Pharmaceuticals就是其中一家。
Inovio选择的是少数人走的治疗性疫苗的道路。
从2008年进入首次人体临床试验算起,VGX-3100的研发之路已经快18年。该疫苗是一款以HPV16/18型病毒的E6和E7蛋白为靶点的DNA疫苗,用于治疗HPV-16/18相关疾病,包括高级別宫颈鳞状上皮内病变(HSIL)。其创新之处在于,采用肌肉注射伴随电脉冲给药的方式,提高DNA 质粒分子进入细胞内的效率,来增强免疫原性。
2015年,Inovio 制药发布 VGX-3100 治疗高级别宫颈肿瘤妇女的IIb期试验结果,所有终点均达到统计学差异。“更广泛地说,这项试验证明在最初未能控制感染的妇女中,提升 HPV 的免疫清除是可能的。” 在评论 Inovio 的 HPV 结果时,美国国家癌症研究所癌症流行病学&遗传学的两位高级研究人员(Schiffman 博士与 Wentzensen 博士)写道。
中国的宫颈癌前病变治疗市场前景广阔,根据弗若斯特·沙利文的分析,中国由HPV-16/18感染引发的宫颈癌前病变患者总数超过700万,其中就诊患者已超过200万人。
东方略敏锐地捕捉到宫颈癌前病变的治疗在中国存在巨大的的未满足的临床需求。2016年,在深入评估VGX-3100的IIb期临床数据后,公司果断决策,以数千万美元的对价获得了该产品在大中华区(涵盖中国大陆、香港、澳门及台湾)的独家开发、生产与商业化权利。
宫颈癌前病变的致病机制清晰,即主要由高危型HPV-16/18持续感染驱动。这促使众多企业围绕该靶点,从不同技术路线展开研发攻关。
在进展较快的产品中,东方略的VGX-3100与亚虹医药的APL-1702代表了两种截然不同的干预路径。APL-1702采用光动力药物与器械相结合的局部治疗方式,直接作用于宫颈病变部位,属于物理治疗的升级。
VGX-3100则是一种全新的治疗范式,通过系统性主动免疫诱导的特异性抗病毒细胞免疫反应,从根源上清除HPV感染和由其引起的病变,实现长期治愈。
HPV治疗性疫苗的技术路线主要包括mRNA载体、DNA载体和腺病毒载体。
与RNA疫苗相比,DNA疫苗具备多方面的突出技术优势。其在热稳定性方面表现更佳,储存与运输条件相对宽松,成本显著降低,也更适合大规模生产。在作用机制上,DNA疫苗可在体内实现更持久的抗原表达,从而诱导更强、更持久的T细胞免疫应答,这对清除由病毒持续感染引起的组织病变具有独特价值。
在递送与安全性方面,DNA疫苗通常采用肌肉注射配合电穿孔技术递送,无需依赖脂质纳米颗粒(LNP)包载,不仅简化了制剂工艺,也降低了由LNP可能引发的炎症反应与过敏风险。
况且,DNA疫苗技术路线的临床可行性已经被验证。2025年,INOVIO开发的另一个DNA 治疗性疫苗INO-3107 向 FDA滚动提交 BLA,即将成为全球首款上市的 DNA 治疗性疫苗。该疫苗针对由HPV-6/11感染引起的复发性呼吸道乳头状瘤病,也是一种此前仅能依靠手术缓解的疾病。INO-3107展现出深度且持久的缓解效果,完全缓解率(CR)由第一年的28%进一步提升至第三年的54%,总缓解率(ORR)则由72%提升至86%。
从临床进展来看,东方略的VGX-3100第一个适应症宫颈癌前病变已经完成III期临床入组和给药,相比仍处于早期阶段的RNA类竞品,确立了至少五年的领先窗口,有望更早占领市场并建立渠道与品牌优势。
作为中国目前唯一同时拥有DNA质粒设计与电脉冲递送系统平台的生物技术公司,东方略在DNA治疗性疫苗领域已经建立起技术与产业壁垒。多年前的布局,正逐步转化为现实的商业价值。
02临床关键数据指向何处?
VGX-3100之所以备受市场瞩目,关键在于其巨大的临床需求和疗效潜力。
VGX-3100两个已完成的三期临床试验的主要终点同时要求组织病理学转归和病毒清除。
这个复合终点的设计同时考虑到了该疾病的病因和临床诊疗实际。病毒清除意味着病因的去除,组织学转归意味着患者可免于手术。
早在2021年3月,INOVIO公布了其关键性III期临床试验REVEAL 1的积极结果:治疗组呈现的有效率明显高于对照组,具有统计学意义,达到主要终点,次要终点也全部达成。
2023年3月,INOVIO公布了另一项Ⅲ期试验Reveal 2的积极数据。分析显示,虽然25名生物标志物阳性患者的疗效终点未达到统计学差异,但在所有参与临床试验的203名患者中,同时实现组织学转归和病毒清除的主要疗效终点达到了统计学显著性差异。
尤其在病毒清除的次要终点,用药组的病毒清除率显著高于安慰剂组。对于患者而言,即便病变组织未完全消退,实现HPV病毒的清除本身也是一项重要的治疗成果。这代表着疾病根本驱动因素的消除,可能从根本上降低病变复发和未来进展为宫颈癌的风险。
长期观察结果也支持VGX-3100作为手术的替代方案:约四成患者在无需手术的情况下病变消退,并在至少1.5年内保持高比例HPV16/18清除和细胞学改善,其长期效果和常规手术相当,有望成为保护生育功能的非手术治疗新选择。
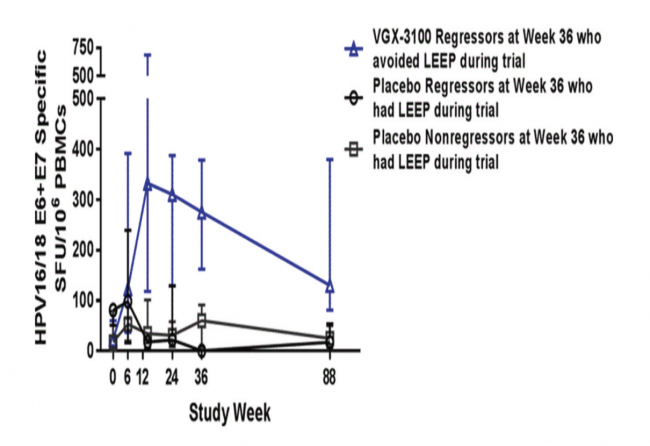
VGX-3100治疗88周后的疗效观察
至此,VGX-3100的临床价值已经得到证明,该疗法有望改变只能物理治疗的现状并进入治疗指南。VGX-3100在两项全球III期临床试验(REVEAL1与REVEAL2)中取得的积极数据,为其在全球多个市场,包括中国市场寻求监管批准提供了重要依据。
在中国市场,东方略在开展的Ⅲ期注册性临床试验在顺利进行中,由中国医学科学院肿瘤医院的吴令英教授牵头,国内22家三甲医院共同开展随机、双盲、安慰剂对照的注册临床研究,现已完成全部患者的入组,展现出的良好安全性与疗效潜力。
东方略也在推进其他适应症的临床审批,于2024年通过VGX - 3100项目针对HPV - 16/18肛门癌前病变的II期临床试验申请,2025年通过针对阴道癌前病变的II期临床试验申请。
弗若斯特·沙利文针对VGX-3100的宫颈、肛门和阴道HSIL三个适应症的销售预测显示,VGX-3100的销售峰值可达到百亿级别。
03 东方略的棋局
如今,东方略旗下核心产品VGX-3100也已被复星医药纳入其战略版图,复星医药获得了该产品在大中华区的独家商业化权益。凭借覆盖全国的销售网络和成熟商业化体系,复星医药有望为VGX-3100的未来上市与市场渗透提供强大引擎,推动该创新疗法更快、更广地惠及中国患者。
对东方略而言,这步“中盘”的加持,为其冲刺阶段提供了至关重要的商业资源与市场背书。借此推力,东方略将进一步开发更多病毒感染导致的疾病适应症,拓展DNA核酸药物技术平台的广度和深度。
东方略的前景正与核心产品的临床结局紧密绑定。随着VGX-3100临床试验揭盲,公司将同时具备产品上市与公司上市申请的关键条件。2026年即将揭晓谜底,这不仅意味着它可能成为全球首款获批的宫颈癌治疗性DNA疫苗,更具有重要的公共卫生意义——2020年,世界卫生组织正式将宫颈癌列为全球首个承诺消除的癌症,VGX-3100的早日获批与应用,将为实现这一全球战略目标提供助力。
编辑:ifhealth 来源:医事药闻
